ESTUDIOS EN
REPRODUCCION ASISTIDA
Desde OMICASLAB, ofrecemos alternativas de estudio que involucran el empleo tanto de gametos propios como donados.
EN GAMETOS PROPIOS
-
HERES – Estudio de portadores
¿En qué consiste este estudio genético?
El HERES de FullGenomics es un test genético exhaustivo en la evaluación de portadores, diseñado para parejas que desean tener un hijo sano, un embarazo seguro. En la actualidad analiza más de 300 enfermedades hereditarias entre las que se seleccionan aquellas con un gran impacto en la esperanza de vida o en su calidad.
Algunas de estas enfermedades son:
-
Fibrosis quística
-
Síndrome de X frágil
-
Atrofia muscular espinal
-
Anemia de células falciformes
-
Alfa y beta talasemia
-
Enfermedad de Tay-Sachs
Lista de enfermedades completa

¿Por qué es importante determinar el riesgo de transmitir una enfermedad genética a su hijo?
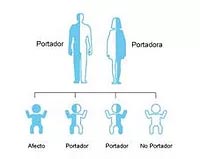
Nuestros genes proporcionan instrucciones a nuestro cuerpo para crecer y funcionar. Todos tenemos dos copias de cada gen. Modificaciones en estos genes, llamadas mutaciones, pueden combinarse en nuestros hijos y causar enfermedades hereditarias que pueden perjudicar en su salud y bienestar.
Los portadores de una enfermedad genética tienen una copia de un gen que no funciona, pero normalmente no presentan problemas de salud y habitualmente carecen de un historial familiar de la enfermedad. Con tan solo una muestra de sangre o saliva, el test Heres de FullGenomics determina si es usted portador de más de 300 enfermedades genéticas y si corre el riesgo de transmitir alguna enfermedad genética a su hijo. Con esta información usted puede planear una familia saludable.
¿Por qué debería realizarme este análisis genético?
Es el único panel que tiene en cuenta las diferencias multiétnicas por lo que puede ser utilizado por todo el mundo independientemente de su procedencia.
-
Personalización de pruebas para integrarse perfectamente con su clínica.
-
Capacidad para agregar nuevas enfermedades y mutaciones con evidencia científica.
-
Examina enfermedades autosómicas recesivas y herencia recesiva ligada al cromosoma X.
-
300 enfermedades y más de 2.000 mutaciones. Detector de portadores más relevante del mundo
-
Tecnología genotipificación/secuenciación de illumina, incluyendo mutaciones intrónicas, exónicas y del promotor
Le ayudamos a entender sus resultados
Asesoramiento genético exhaustivo pre y pos-test por técnicos con formación avanzada específica facilitando la toma de decisión tras el resultado, comprometiéndonos así a ofrecerle información, orientación, y apoyo durante todo el proceso. Nuestros asesores de genética le ayudarán a interpretar los resultados de la prueba Heres dentro del marco de su historial médico, ayudándole a tomar decisiones médicas y reproductivas basadas en sus resultados.
-
EN GAMETOS DONADOS
-
FENOMATCH Encuentra tu donante ideal

AUMENTA LA POSIBILIDAD DE QUE TU HIJO SE PAREZCA A TI

El reconocimiento facial de Fenomatch te ofrece la herramienta que necesitas
Actualmente, ante los casos de donación de gametos, las clínicas de fertilidad buscan en los bancos de óvulos/esperma un donante que cumpla los criterios de calidad y cantidad adecuados. Sin embargo, en cuanto a los criterios fenotípicos, únicamente seleccionan características básicas como el color de pelo, etnia o color de ojos. Gracias a FenoMatch, las clínicas de fertilidad pueden profundizar en la selección de donantes de manera más exhaustiva, eligiendo entre todos los candidatos donantes el que más se parezca a la persona o pareja receptora. Esta herramienta no solo selecciona y ordena los donantes según su parecido fenotípico, sino que además es capaz de comparar los resultados de pruebas genéticas de enfermedades hereditarias para eliminar la incompatibilidad genética entre los posibles donantes y la persona o pareja receptora.
Fenomatch busca donantes que se parezcan a ti o a tu pareja

Mediante algoritmos de BigData, esta herramienta estudia más de 100 puntos faciales y las distancias entre ellos para determinar con una puntuación del 1 al 100 el grado de parecido donante/receptor, seleccionando el donante que tenga una puntuación más alta. Este algoritmo, denominado FenoMatch Score, permite ordenar por parecido a los distintos usuarios, adaptando la escala en base a saltos de etnia, color de piel, etc. Este score va desde 1 (no se parece nada) hasta 100 (se considera que son la misma persona o un hermano gemelo). Asimismo, con técnicas BigData, esta herramienta puede también comparar los resultados de pruebas genéticas de enfermedades hereditarias, sabiendo, para determinadas enfermedades si la conjunción donante-paciente tiene un alto o bajo riesgo de transmisión.
Alta fiabilidad de los resultados

Fenomatch ofrece tres tipos de matching distintos:
-
Pre-matching fenotípico: permite introducir una serie de prefiltros relacionados con el aspecto físico principalmente, así como la estatura, el color de pelo, el grupo sanguíneo, el color de ojos, complexión, etc.
-
Pre-matching genético: compara los resultados de pruebas genéticas de enfermedades hereditarias, sabiendo, para determinadas enfermedades, si la conjunción donante-paciente tiene un alto o bajo riesgo de transmisión.
-
Matching facial: tras eliminar de forma automática los donantes que no encajen en los pre-matching anteriores, se realizará la comparación de similitud entre la cara del paciente y la de los posibles donantes a partir de las fotografías faciales de estos, estudiando más de 100 puntos faciales y la distancia entre ellos. Finalmente, los donantes candidatos serán ordenados según el parecido y el índice de importancia de los pre-matching anteriormente realizados.
De esta manera, se consigue obtener el donante que más se parece al paciente al comparar la puntuación de todos los pares de imágenes disponibles, que anteriormente, si se desea, han sido preseleccionados siguiendo unos criterios fenotípicos y genotípicos. Finalmente, el médico podrá contar con un listado de donantes óptimos para cada caso, prevaleciendo siempre el criterio del profesional para la selección del donante final.
-
-
Estudio de portadores
¿En qué consiste este estudio genético?
El estudio de portadores es un test genético exhaustivo en la evaluación de portadores, diseñado para parejas que desean tener un hijo sano, un embarazo seguro. En la actualidad analiza más de 300 enfermedades hereditarias entre las que se seleccionan aquellas con un gran impacto en la esperanza de vida o en su calidad.
Algunas de estas enfermedades son:
- Fibrosis quística
- Síndrome de X frágil
- Atrofia muscular espinal
- Anemia de células falciformes
- Alfa y beta talasemia
- Enfermedad de Tay-Sachs
Lista de enfermedades completa: carrier_screening_test-_disease_list_OMICAS
¿Por qué es importante determinar el riesgo de transmitir una enfermedad genética a su hijo?
Nuestros genes proporcionan instrucciones a nuestro cuerpo para crecer y funcionar. Todos tenemos dos copias de cada gen. Modificaciones en estos genes, llamadas mutaciones, pueden combinarse en nuestros hijos y causar enfermedades hereditarias que pueden perjudicar en su salud y bienestar.
Los portadores de una enfermedad genética tienen una copia de un gen que no funciona, pero normalmente no presentan problemas de salud y habitualmente carecen de un historial familiar de la enfermedad. Con tan solo una muestra de sangre o saliva, este estudio es capaz de determinar si es usted portador de más de 300 enfermedades genéticas y si corre el riesgo de transmitir alguna enfermedad genética a su hijo. Con esta información usted puede planear una familia saludable.

¿Por qué debería realizarme este análisis genético?
Es el único panel que tiene en cuenta las diferencias multiétnicas por lo que puede ser utilizado por todo el mundo independientemente de su procedencia.
-
Personalización de pruebas para integrarse perfectamente con su clínica.
-
Capacidad para agregar nuevas enfermedades y mutaciones con evidencia científica.
-
Examina enfermedades autosómicas recesivas y herencia recesiva ligada al cromosoma X.
-
300 enfermedades y más de 2.000 mutaciones. Detector de portadores más relevante del mundo
-
Tecnología genotipificación/secuenciación de illumina, incluyendo mutaciones intrónicas, exónicas y del promotor
Le ayudamos a entender sus resultados
Asesoramiento genético exhaustivo pre y pos-test por técnicos con formación avanzada específica facilitando la toma de decisión tras el resultado, comprometiéndonos así a ofrecerle información, orientación, y apoyo durante todo el proceso. Nuestros asesores de genética le ayudarán a interpretar los resultados del estudio dentro del marco de su historial médico, ayudándole a tomar decisiones médicas y reproductivas basadas en sus resultados.
ESTUDIOS EN EL EMBRIÓN
-
PGT-EM Test genético de preimplante para enfermedades monogénicas
TEST GENÉTICO DE PREIMPLANTE PARA ENFERMEDADES MONOGÉNICAS (PGT-EM)
Existen diversas enfermedades resultado de mutaciones genéticas específicas en el ADN. Las personas o parejas que portan estas alteraciones genéticas, o que tengan familiares que las posean, tendrán un mayor riesgo de tener un hijo afectado por esta alteración. El PGT-EM se encarga de buscar en el embrión posibles alteraciones genéticas que hayan sido identificadas previamente en los progenitores para evitar su transmisión a la descendencia.
Esta técnica puede identificar previamente a la transferencia, los embriones que estén libres de estas anomalías, con el objeto de lograr el nacimiento de un bebé que no posea la alteración genética y reduciendo además la posibilidad de aborto.
Esta técnica está dirigida a parejas que se encuentran en riesgo de transmitir a sus hijos una determinada enfermedad monogénica, o trastorno genético único, siempre y cuando haya sido identificado previamente en los progenitores.
El PGT-EM es aplicable en los siguientes escenarios:
- Parejas de portadores con una misma afección autosómica recesiva (por ejemplo, fibrosis quística).
- Portador de una afección ligada a X (por ejemplo, distrofia muscular de Duchenne).
- Pacientes con una afección autosómica dominante (por ejemplo, enfermedad de Huntington).
- Pacientes con una mutación asociada con un síndrome de cáncer hereditario (por ejemplo, BRCA1 y 2).
- Parejas con un hijo o un embarazo con un desorden monogénico.
¿Cómo se realiza un PGT-EM?
Para llevar a cabo esta técnica, la paciente debe someterse en primer lugar a un ciclo de fecundación in vitro. Posteriormente, los óvulos fecundados obtenidos son cultivados en el laboratorio durante varios días, después de los cuales se les realiza una biopsia embrionaria mediante la cual se extrae cuidadosamente un grupo de células.
A continuación, se efectúa el estudio genético correspondiente en este material biopsiado, permitiendo identificar mediante NGS, aquellos embriones portadores de las anomalías genéticas analizadas, transfiriendo posteriormente los que estén libres de estas alteraciones.
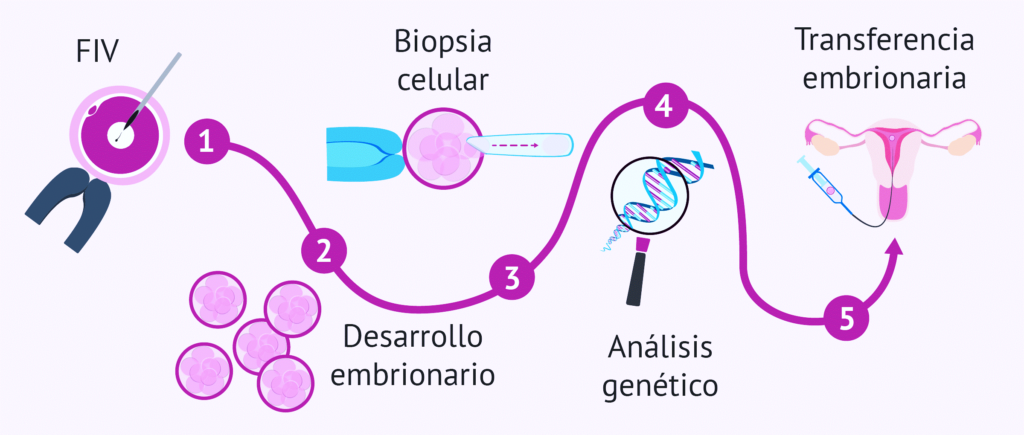
FUENTE IMAGEN: https://www.reproduccionasistida.org/procedimiento-del-dgp/
-
PGT-A Test genético de preimplante para aneuploidias
TEST GENÉTICOS DE PREIMPLANTACIÓN EMBRIONARIA (PGT)
Las pruebas genéticas de preimplantación, son técnicas de última generación en las que se realiza un estudio genético en el embrión antes de su implantación en el útero materno, con el objetivo de seleccionar aquellos embriones libres de determinadas alteraciones genéticas o cromosómicas.
Hasta hace poco tiempo, se los conocía como PGS (Screening genético de preimplante) y en PGD (Diagnóstico genético de Preimplante)
Hoy se los clasifica como:
-
PGT-A Test Genético de Preimplante para Aneuploidías
-
PGT-EM Test Genético de Preimplante para Enfermedades Monogénicas
TEST GENÉTICO DE PREIMPLANTE PARA ANEUPLOIDIAS (PGT-A)
El embrión humano está compuesto por 23 pares de cromosomas, un par heredado de la madre y otro del padre. Esta cantidad normal de cromosomas es conocida como euploidía. Sin embargo, existen embriones que presentan un defecto o exceso de cromosomas, lo que se conoce como aneuploidías cromosómicas. Estas aneuploidías, además de desempeñar un papel en algunas enfermedades, pueden aumentar la probabilidad de aborto involuntario y ser la causa del fracaso de las técnicas de reproducción asistida en muchas mujeres. El PGT-A es una técnica que permite estudiar todos los cromosomas presentes en el embrión, permitiendo identificar si los embriones poseen un número correcto de cromosomas o si existen anomalías cromosómicas en los mismos. Las aneuploidías son variaciones numéricas del complemento cromosómico normal de la célula (mayor o menor a 46). Las aneuploidías más frecuentes se deben a la presencia de un cromosoma de más (trisomía) o de menos (monosomía), de forma total o parcial, en uno o más cromosomas
Para llevar a cabo esta técnica, se emplea la secuenciacion masiva, una tecnología que permite identificar todos los cromosomas de forma rápida y eficaz. De esta manera, mediante el PTG-A se consigue seleccionar aquellos embriones cromosómicamente normales, consiguiendo aumentar las tasas de embarazo. Esta técnica se utiliza en casos de fallos de implantación, abortos de repetición, anomalías cromosómicas en embarazos anteriores, edad materna avanzada o alteraciones graves en los espermatozoides.
Las afecciones comunes causadas por anomalías cromosómicas incluyen, entre otras:
-
Síndrome de Down
-
Síndrome de Turner
-
Síndrome de Klinefelter.
¿Cómo se realiza un PGT-A?
Para llevar a cabo esta técnica, la paciente debe someterse en primer lugar a un ciclo de fecundación in vitro. Posteriormente, los óvulos fecundados obtenidos son cultivados en el laboratorio durante varios días y se les realiza una biopsia embrionaria mediante la cual se extrae cuidadosamente un grupo de células del embrión. A continuación, mediante secuenciacion masiva, se realiza el estudio genético correspondiente en este material biopsiado, permitiendo identificar aquellos embriones que poseen anomalías cromosómicas. Finalmente, aquellos embriones que no posean ninguna de estas anomalías, son transferidos al útero materno.
-
